Contoh Soal Penurunan Titik Beku – Membahas mengenai perhitungan suatu proses kimia terkait zat berbentuk larutan. Dimana reaksi penurunan titik beku tersebut terjadi pada saat suatu larutan saat ditambahkan senyawa lain.
Jika dilihat dari sudut pandang ilmu kimia, larutan mempunyai berbagai sifat baik dalam bentuk sifat kimia ataupun sifat fisis. Dimana salah satu materi sifat fisis tersebut dipelajari di saat seorang siswa SMA ataupun MA menginjak kelas 12 yakni sifat koligatif.
Sifat koligatif sendiri merupakan sebuah sifat larutan kimia yang berubah secara fisis akibat partikel zat terlarut di dalam sebuah pelarut pada kondisi tertentu. Sifat koligatif terbagi menjadi 4 (empat) kondisi, dimana salah satunya adalah penurunan titik beku.
Pada kesempatan kali ini, Kursiguru akan membahas secara khusus mengenai penurunan titik beku (ΔTf) beserta contoh soalnya. Dimana Penurunan titik beku sendiri bisa dihitung apabila data molalitas larutan dan koefisien penurunan titik beku sudah diketahui.
Pengertian Penurunan Titik Beku
Sebelum membahas seputar contoh soal penurunan titik beku, penulis akan menjelaskan terlebih dahulu tentang materi dasar terkait penurunan titik beku. Untuk mempersingkat waktu silakan simak langsung pembahasan tentang penurunan titik beku berikut.
Titik Beku
Bahasan pertama adalah mengenai titik beku, dimana titik beku atau freezing temperature (Tf) adalah nilai suhu ketika cairan serta zat padat berada pada kondisi tekanan uap sama. Sebagai salah satu contoh adalah titik beku air, yaitu 0°C (nol derajat Celsius).
Apabila titik beku didapatkan saat zat cair serta zat padat berada dalam kondisi setimbang (1 atm atau 760 mmHg) maka akan disebut dengan istilah titik beku normal. Berikut adalah gambaran kondisi titik beku (Kf) untuk beberapa jenis pelarut.
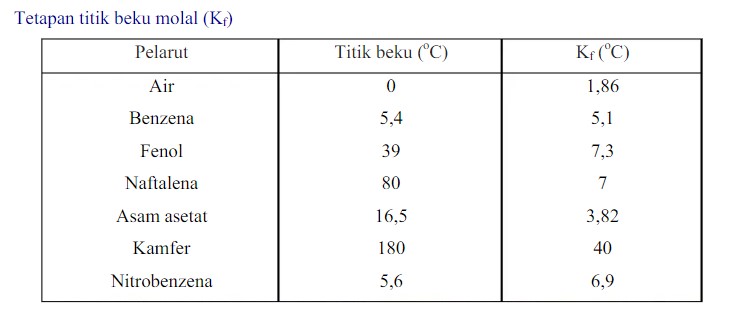
Penurunan Titik Beku
Saat ada sebuah senyawa terlarut dimasukkan ke dalam pelarut sehingga menyebabkan penurunan tekanan uap jenuh larutan ke titik tertentu. Ketika tekanan uap jenuh itu mengalami penurunan, secara otomatis akan terjadi penurunan titik beku menjadi di bawah titik beku normalnya.
Penurunan titik beku juga termasuk selisih antara titik beku pelarut dengan titik beku larutan, kondisi penurunan titik beku termasuk salah satu dari sifat koligatif larutan. Dalam penghitungan kimia, penurunan titik beku memiliki simbol ΔTf (f berasal dari kata freeze) atau ΔTb.
Penerapan Penurunan Titik Beku
Penurunan titik beku juga sering dipakai dalam kehidupan sehari-hari, hal tersebut berlaku untuk pembuatan makanan sampai kendaraan. Untuk lebih mempermudah memahami penerapan penurunan titik beku, silahkan lihat penjelasan berikut.
1. Pembuatan Ice Cream
Penerapan titik beku juga diterapkan pada pembuatan ice cream, dengan cara menambahkan garam pada es, dengan tujuan agar suhu lebih turun. Apabila suhu tidak diturunkan, maka air dalam adonan ice cream tidak dapat membeku. Hasilnya ice cream pun tidak mengeras.
2. Mencairnya Salju
Musim dingin selalu di identikan dengan sebuah salju serta udara dingin. Pada saat salju turun dengan lebat, maka hal tersebut akan menutupi jalan atau benda lain. Untuk mengatasi hal tersebut ialah dengan cara mencairkan salju menggunakan garam.
Air dapat membeku pada saat suhu 0 derajat celcius. Apabila ditambahkan garam, maka hal tersebut akan menurunkan suhu. Semakin tinggi konsentrasi dari garam, maka akan semakin rendah titik beku air. Oleh karena itu, suhu salju dapat menurun sehingga akan cair nantinya.
3. Air Laut
Pada saat musim dingin, air laut tidak seluruhnya membeku. Hal tersebut dikarenakan kadar garam pada air laut berbeda-beda, dengan begitu suhu setiap air laut akan berbeda-beda. Semakin tinggi kadar garam pada air laut, maka penurunan titik beku pada air laut tersebut akan semakin tinggi.
Rumus Penurunan Titik Beku
Agar dapat menghitung penurunan titik beku tentunya kamu memerlukan persamaan atau rumus perhitungannya. Oleh karena itu, di sini penulis akan membagikan rumus penurunan titik beku seperti pada gambar berikut ini.

Contoh Soal Penurunan Titik Beku
Setelah mengetahui dasar materi beserta rumusnya, silakan simak langsung contoh soal turunnya titik beku dari Kursiguru berikut. Dimana tiap contoh soal penurunan titik beku di bawah masing-masing disertai jawaban serta pembahasan.
Contoh Soal (1)
Frozon mempunyai beberapa jenis larutan yakni:
– glukosa 0,05M
– glukosa 0,10M
– sukrosa 0,10M
– sukrosa 0,15M
– urea 0,15M
Jelaskan solution milik Frozon mana yang mempunyai titik beku paling tinggi!
Jawaban :

Contoh Soal (2)
Jika Andrew mempunyai larutan ethanol (solution) dengan massa sebesar 30% di dalam air, maka berapakah nilai molalitasnya? (Mr = 46 gram/mol)
Jawaban :

Contoh Soal (3)
Dr. Brooks melarutkan 18 gram glukosa (C6H12O6) ke dalam 500 gram air. Jika kalor beku molal air Kf= 1,8/mol (Ar:C=12 g/mol, H=1 g/mol, O=16 g/mol), maka titik bekunya berada pada suhu berapa?
Jawaban :

Contoh Soal (4)
Singsing memiliki 300 gram air, dimana didalamnya terlarut terdapat 40 gram zat X. Jika larutan tersebut membeku pada suhu -3,1°C. Apabila Kf air = 1,86°C, maka Mr zat X tersebut mempunyai nilai sebesar?
Jawaban :

Contoh Soal (5)
Dr. Vegapunk mempunyai larutan yang terdiri dari 12 gram zat X (non elektrolit) serta 20 gram air. Jika Mr zat X adalah 223, maka akan terjadi penurunan titik beku sebesar? (Kf = 1,86°C)
Jawaban :

Itulah beberapa contoh soal terkait salah satu komponen sifat koligatif kimia yakni penurunan titik beku. Dimana 10 contoh soal penurunan titik beku lainnya bisa disimak pada file PDF di bawah.
Selain itu, penurunan titik beku tersebut akan berpatokan pada titik beku normal pada kondisi setimbang. Jadi agar lebih memahami penurunan titik beku, sebaiknya kamu pelajari juga contoh soal kesetimbangan kimia.
Download Contoh Soal Penurunan Titik Beku
Untuk melengkapi bahasan di atas, di sini Kursiguru juga hendak membagikan file kumpulan soal terkait penurunan titik beku. Silakan download langsung file PDF soal penurunan titik beku di bawah tanpa perlu ragu karena penulis sediakan secara gratis.
Perlu diketahui pula bahwa untuk jenjang SMA atau sederajat, soal-soal penurunan titik beku biasanya fokus kepada jenis larutan non elektrolit. Sementara terkait penurunan titik beku larutan elektrolit akan dibahas pada jenjang perguruan tinggi.
Akhir Kata
Demikian bahasan Kursiguru seputar materi penurunan titik beku kimia kelas 12 beserta rumus, contoh soal serta jawaban dan pembahasannya. Semoga dapat membantu proses belajar ataupun persiapan ujian semua siswa SMA serta MA.

